Günstiger Zelltröpfchendrucker
Produktübersicht: 3D-Zellkultursysteme
Alle Produkte im Überblick 
Vorgefertigte Platten und Schalen mit speziellen Oberflächenstrukturen erleichtern die dreidimensionale Kultur von Zellen. Zelldichten wie in natürlichem Gewebe erzeugt ein neuentwickelter Biodrucker.
Wer von den üblichen zweidimensionalen adhärenten Zellkulturen auf dreidimensional (3D) wachsende Kulturen umsteigen möchte, kann mittlerweile aus einer großen Palette an 3D-Zellkultursystemen auswählen. Am reibungslosesten dürfte der Wechsel für 3D-Zellkultur-Novizen mit Sphäroid-Systemen funktionieren.
Sphäroide sind kleine kugelförmige Zellhaufen, deren Durchmesser meist zwischen 30 und 50 Mikrometern liegt, aber auch über 500 Mikrometer erreichen kann. Da in den kleinen Zellkugeln ähnliche Konzentrationsgradienten vorliegen, etwa im Gehalt von Nährstoffen, Sauerstoff oder Metaboliten, wie in soliden Tumoren, sind sie insbesondere bei Krebs- und Wirkstoffforschern als Modell-Systeme sehr gefragt. Ihre Herstellung ist vergleichsweise simpel und erfolgt meist in den Näpfchen spezieller Mikrotiterplatten.
Die Plattenhersteller setzen in der Regel zwei einfache Tricks ein, mit denen sie die Zellverbände dazu bringen, kugelförmig zu wachsen. Erste Voraussetzung ist eine aalglatte Oberfläche, an der selbst Adhäsionskünstler unter den Zellen nicht anhaften können. Dies reicht für die Ausbildung eines wohlgeformten Sphäroids jedoch noch nicht aus. Dazu muss auch die Geometrie des Näpfchenbodens stimmen. Die Platten-Hersteller bieten häufig RundwellPlatten an, deren Wellböden nicht eben, sondern nach außen gewölbt sind. Wird die Zellsuspension in die Näpfchen pipettiert, sammeln sich die Zellen in der runden Vertiefung an und bilden Sphäroide.
Gefährliche Zellcluster
Häufig wachsen diese in den einzelnen Näpfchen jedoch nicht ganz gleichmäßig heran. Einige sind größer oder bilden unregelmäßig geformte Zellcluster, die dazu tendieren, an der Plattenoberfläche anzuhaften. In der Grundlagenforschung mag dies noch durchgehen. Bei Stammzell-Sphäroiden, die für Zell-Transplantation gezüchtet werden, sind diese Unregelmäßigkeiten jedoch unerwünscht. Zu groß ist das Risiko, dass sich einzelne Zellen zu Tumoren weiterentwickeln.
Vor diesem Problem stand auch der Schweizer Chirurg Patrick Kugelmeier. Kugelmeier arbeitete während seiner Ausbildung an der Universität Zürich daran, die komplizierte und häufig nicht erfolgreiche Transplantation der Bauchspeicheldrüse durch die einfachere Transplantation von Langerhansschen Inselzellen zu ersetzen. Für die Transplantationen benötigte er Inselzell-Sphäroide mit einer exakt definierten Größe (zu große werden nach der Transplantation abgestoßen), die er möglichst schnell und einfach in großen Mengen herstellen konnte.
Eigentlich ziemlich simple Vorgaben, an denen die bestehenden kommerziellen Sphäroid-Systeme jedoch allesamt scheiterten. Der Mediziner entschloss sich deshalb, eigene Sphäroid-Platten zu entwickeln und ließ diese 2011 patentieren.
Die Form der Näpfchen entspricht in seinen Platten einer auf dem Kopf stehenden Pyramide mit quadratischer Grundfläche. Dies ist zunächst nichts Besonderes. Auf die Idee, die Wellböden in Pyramiden-Form auszuführen, kamen auch schon andere Hersteller. Kugelmeiers Pyramiden-Näpfchen enden jedoch nicht wie üblich in einer scharfkantigen Spitze, sondern in einer Rundung. Diese kleine Modifikation führt dazu, dass die Zellen in sämtlichen Wells zu sehr einheitlichen Sphäroiden heranwachsen, die der Experimentator in der jeweils gewünschten Größe ernten kann. Die Platten sind insbesondere für die Kultur von Stammzell-Sphäroiden gedacht, es spricht aber nichts dagegen, sie auch für die dreidimensionale Kultur anderer Zellen einzusetzen.
Neben den weiteren, beinahe schon klassischen Methoden der 3D-Zellkultur mithilfe von Trägern (Scaffolds) oder Hydrogelen experimentieren Forscher auch mit 3D-Biodruck-Verfahrern. Eine sowohl kostengünstige als auch interessante neue Bioprinting-Technik stellte die Gruppe des englischen Chemikers Hagan Bayley von der Universität Oxford im August vor (Scientific Reports 7: 7004).
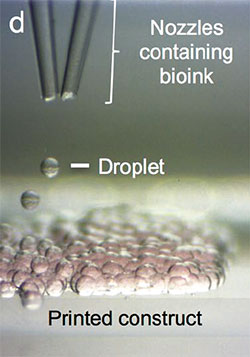
Der Spezialist für Membranporen-Proteine entwickelte ein ebenso cleveres wie einfaches, Tropfen-basiertes Biodruck-Verfahren. Bei diesem sprüht der Drucker aus einer kleinen Düse winzige Tropfen einer Zellsuspension mit einem Volumen von einem Nanoliter und etwa 130 Mikrometer Durchmesser in ein ölgefülltes Gefäß mit einer Glasoberfläche (siehe Bild oben). Ein motorisierter Mikromanipulator bewegt den Ölbehälter an die gewünschten Koordinaten. Bayleys Trick besteht darin, Lipide in das Öl zu mischen, die sofort eine Lipid-Einfachschicht um jeden Tropfen bilden, der in das Öl fällt. Nähern sich die Tropfen einander an, schließen sie sich – stabilisiert durch entstehende Lipid-Doppelschichten – zu größeren Verbänden zusammen. Diese bedecken zunächst den Boden des Gefäßes und wachsen schließlich an den gewünschten Positionen auch in der dritten Dimension weiter. Die gedruckten Zellstrukturen verpackten die Engländer in einer Gelschicht und überführten sie nach Entfernen des Öls in Zellkulturmedium, um sie weiter zu kultivieren.
Zelltröpfchen in Öl
Die Auflösung der Tröpfchendruck-Technik aus Bayleys Labor ist deutlich höher als bei gängigen Extrusions-Druckern, welche die Zellen als Strang wie aus einer Tube herausdrücken; und ähnlich gut wie bei Tintenstrahl-Druckern, die Zelltröpfchen mit fünf bis fünfzig Mikrometer Durchmesser ausstoßen. Entscheidender ist jedoch die wesentlich höhere Zelldichte in den Tropfen des englischen Druckers, die wie in natürlichen Zellgeweben bei etwa 30 Millionen Zellen pro Milliliter liegt.
Ein weiterer Vorteil: Der Bioprinter kann zwei verschiedene Zelltypen an beliebigen Positionen der Zell-Konstrukte unterbringen. Mit einem mehrdüsigen Dispenser wäre es sogar möglich, mehr als nur zwei verschiedene Zelltypen in den gedruckten Geweben zu deponieren.
Interessant ist auch der Preis des Druckers. Nach Angaben der Briten liegen die Herstellungskosten deutlich unter 10.000 Euro – und damit am unteren Ende der Preisskala für kommerzielle 3D-Biodrucker. Bayley hat auch schon eine Firma (OxSyBio) gegründet, die sich um die Weiterentwicklung seines Druckers kümmert. Das ist übrigens schon die zweite Firmengründung von Bayley. Der Chemiker legte Ende der neunziger Jahre mit seinen Arbeiten zu Poren-Proteinen die Grundlagen für die Nanoporen-Sequenzierung. Kurze Zeit später gründete er die Firma Oxford Nanopores, die mit ihren MinION-Geräten gerade den Sequenziermarkt aufmischt.
Alle Produkte im Überblick 
(Erstveröffentlichung: H. Zähringer, Laborjournal 10/2017, Stand: Oktober 2017, alle Angaben ohne Gewähr)
Letzte Änderungen: 11.10.2017